生命科学与技术学院高绍荣/陈嘉瑜/江赐忠/姚红杰团队合作研究揭示DDX5维持卵母细胞RNA稳态的分子机制,成果发表于《自然·通讯》
来源:生命科学与技术学院
时间:2026-03-27 浏览:
哺乳动物卵母细胞发育是一个跨越漫长时间维度的复杂过程,其核心任务之一是生发泡(GV)期需要合成大量母源RNA与蛋白质,这些物质一部分用于支持卵母细胞后续成熟,另一部分则被储存在线粒体相关核糖核酸蛋白结构域(MARDO)和胞质晶格结构中,以支持受精后合子基因组激活前的早期胚胎发育。随着转录积累逐渐完成,卵母细胞发生染色质重塑,核构型由非环绕核仁(NSN)转变为环绕核仁(SN),随后恢复减数分裂。RNA结合蛋白(RBP)在上述过程中发挥关键调控作用,但目前被鉴定的RBP有限,整体调控网络仍不清晰。RNA解旋酶DDX5是DEAD-box家族核心成员,已在其他体系中被证实广泛参与RNA代谢过程。在小鼠卵母细胞中,DDX5呈现高表达,然而,它在哺乳动物雌性生殖中所扮演的角色有待阐明。
近日,同济大学生命科学与技术学院高绍荣/陈嘉瑜/江赐忠团队联合广州实验室姚红杰团队在《自然·通讯》(Nature Communications)在线发表题为“DDX5 orchestrates RNA homeostasis to ensure oocyte developmental competence”的研究论文,首次系统揭示了DDX5在卵母细胞发育过程中协调RNA稳态的分子机制。

该研究通过Ddx5f/f;Gdf9-Cre条件性敲除小鼠发现,DDX5缺失导致GV期卵母细胞核构型NSN-SN转变失败,并呈现异常固缩的染色质状态,在本研究中被定义为Failed-SN(FSN)核构型;大部分卵母细胞无法恢复减数分裂,即使发生GVBD的卵母细胞表现为纺锤体组装异常、非整倍体发生率增加,进而无法受精导致雌鼠完全不育。
接着,该研究通过体内外实验,联合Total RNA-seq、ATAC-seq、RIP-seq多组学分析,从mRNA转录、mRNA存储以及逆转座子RNA清除三个维度揭示了DDX5维持卵母细胞RNA稳态的分子机制:1)DDX5在NSN构型GV期卵母细胞中与RNA聚合酶II相互作用以促进活跃转录,其缺失导致转录起始受限,mRNA产量显著降低,并伴随广泛的转录组失调。2)DDX5缺失损害mRNA核输出过程,导致其在核内大量滞留。同时,被运输至胞质的mRNA则由于线粒体排布异常、线粒体膜电位降低、MARDO相关基因下调表达等因素使其未能在MARDO被高效存储,进而发生过度翻译,进一步加剧mRNA耗竭。3)在卵母细胞正常生长过程中,以LTR和LINE为主的逆转座子转录本发生大规模降解,DDX5对这部分逆转座子转录本具有直接结合并促进其清除的作用。卵巢质谱数据发现DDX5和多个外切体相关蛋白(例如MTR4、DIS3、ZC3H18、SRRT等)存在互作,DDX5缺失卵母细胞中上调的逆转座子RNA和外切体RNase活性亚基EXOSC10或DIS3缺失卵母细胞中上调的逆转座子RNA存在大量重叠,说明DDX5可能在该过程上游发挥作用,例如通过其解螺旋功能对需要进行降解的逆转座子转录本进行预处理,进而传递至外切体进行降解。DDX5缺失后,冗余的LTR/LINE RNA导致临近的基因表达上调,进一步对整体转录环境造成干扰。
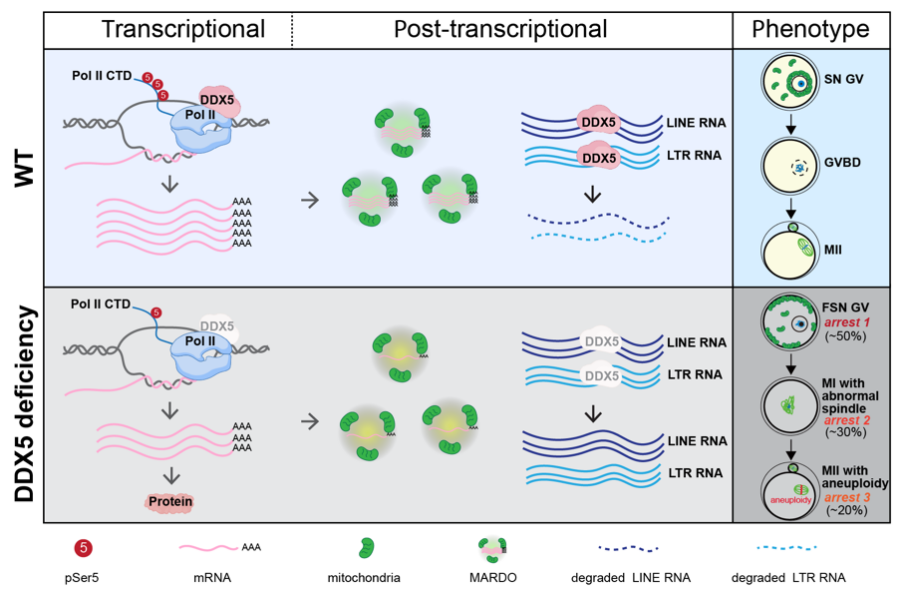
综上所述,这项研究工作不仅从mRNA层面揭示了DDX5在转录及转录后调控中的功能,更从逆转座子RNA清除这一新视角切入,为理解卵母细胞发育机制提供了重要启示,确立了DDX5作为卵母细胞发育和雌性生殖关键调控因子的核心地位。
同济大学生命科学与技术学院陈嘉瑜教授、高绍荣院士、江赐忠教授以及广州实验室姚红杰研究员为论文共同通讯作者。同济大学生命科学与技术学院博士后王梦婷、博士后王莉萍、中国科学院广州生物医药与健康研究院博士后蔡青青为论文共同第一作者。
高绍荣团队与姚红杰团队长期深耕合作,持续揭示DDX5在细胞命运决定中的关键作用。自2017年在Cell Stem Cell首次合作揭示DDX5在体细胞重编程中的作用,到2021年进一步阐明其在原始生殖细胞分化中的重要功能,此次在雌性生殖领域取得的新成果,是双方协同攻关的又一力作。系列研究的持续产出离不开两支团队持之以恒的坚持与紧密无间的协作,期间双方共同承担了两项科技部项目,为深入研究提供了有力支撑。
论文链接:https://doi.org/10.1038/s41467-026-70237-1