生命科学与技术学院高绍荣团队揭示异常的组蛋白二价修饰对体细胞核移植胚胎合子基因激活过程产生影响的机制,成果发表于《蛋白质与细胞》
来源:生命科学与技术学院 时间:2025-03-03 浏览:
体细胞核移植(somatic cell nuclear transfer,SCNT)技术,又称“克隆技术”,通过将终末分化的体细胞核注入去核的卵母细胞获得重构胚胎,从而实现细胞全能性获得重塑。然而,核移植胚胎发育潜能的低下仍然是该项技术广泛应用的主要阻碍。在细胞从终末分化到全能性状态的转变过程中,必然经历复杂且剧烈的表观遗传修饰重编程。因此,深入解析核移植胚胎发育过程中表观修饰的重编程机制及多种修饰之间的相互调控网络,能够为修复核移植胚胎中的表观修饰异常并提高核移植效率提供重要的理论依据。
近日,同济大学生命科学与技术学院高绍荣/李翀/刘晓雨团队在《蛋白质与细胞》(Protein & Cell)杂志上发表题为“Setd2 overexpression rescues bivalent gene expression during SCNT-mediated ZGA”的研究论文。该研究首次描绘了小鼠体细胞核移植胚胎发育过程中组蛋白H3K4me3和H3K27me3修饰的动态变化图谱,揭示了二价修饰(即同时被H3K4me3和H3K27me3修饰所标记)的异常及二价基因的表达失调。研究进一步解析了Setd2作为组蛋白H3K36me3修饰的甲基转移酶,如何在核移植胚胎发育过程中对多种组蛋白修饰进行复杂调控,为进一步提高体细胞核移植效率拓展了全新视野。

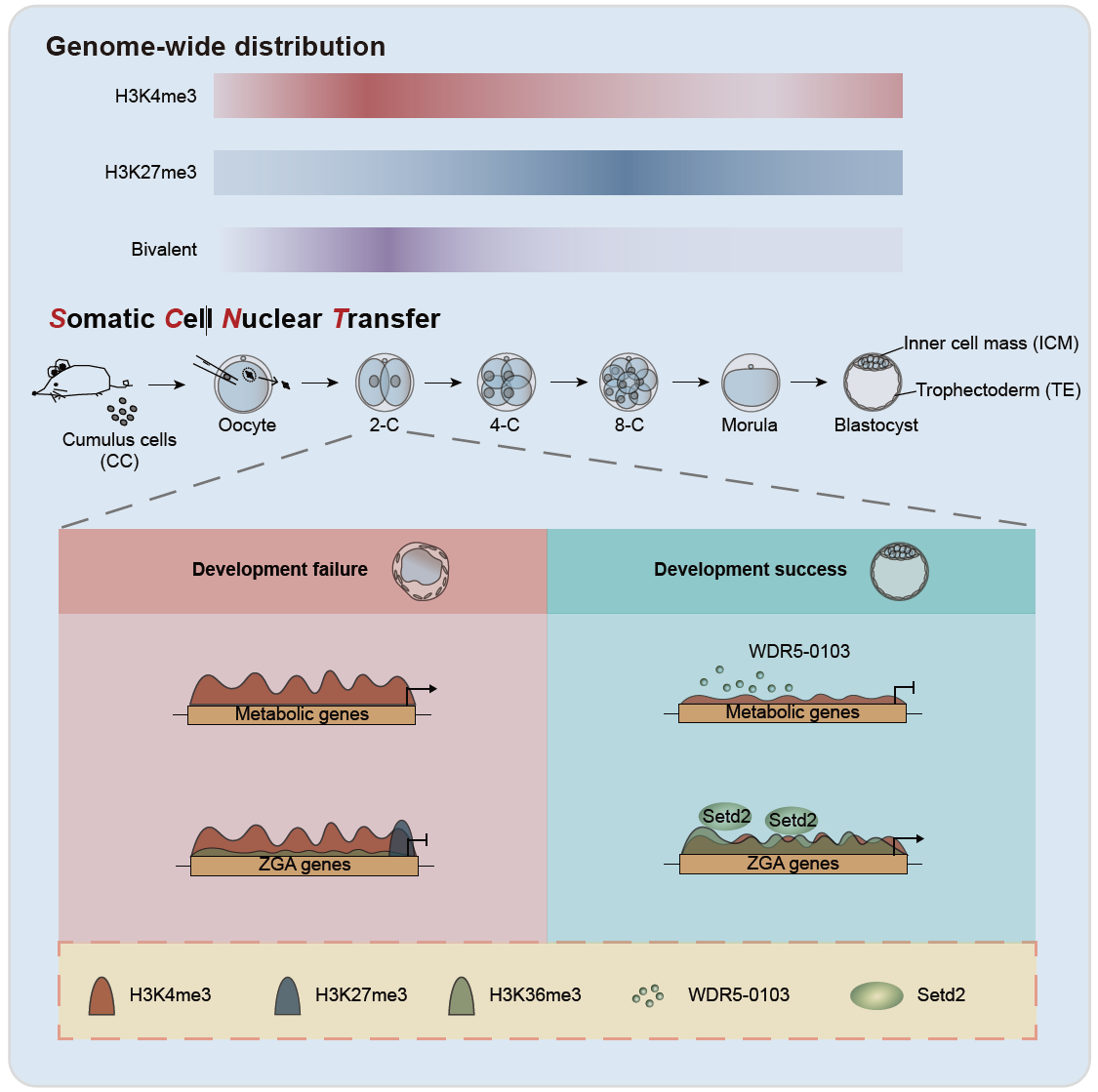
该研究首次绘制了小鼠核移植胚胎发育过程中组蛋白H3K4me3和H3K27me3修饰的动态变化图谱,揭示了这两种修饰在全基因组水平及启动子区的修饰异常。研究发现,与自然受精胚胎相比,核移植胚胎在合子基因激活期(zygotic genome activation,ZGA,发生在小鼠植入前胚胎2-细胞期),组蛋白H3K4me3和H3K27me3修饰在启动子区均出现了异常的过度富集。通过在核移植胚胎中加入组蛋白H3K4me3修饰的小分子抑制剂WDR5-0103,显著提高了核移植胚胎的囊胚率和植入率,同时成功修复了因H3K4me3过度建立而引起的基因表达异常。
进一步的研究发现,在核移植胚胎发育的ZGA时期,二价修饰也存在过度建立的现象,这一现象主要由H3K27me3修饰的异常建立所引起,且二价基因表达水平显著低于同时期自然受精胚胎。通过互斥性分析,研究人员发现,二价修饰的过度建立可能与组蛋白H3K36me3修饰的建立不足相关。为此,研究人员通过过表达H3K36me3的甲基转移酶Setd2,显著提高了核移植胚胎的囊胚率,修复了多种组蛋白修饰的异常,并成功挽回了二价基因的表达异常。
综上所述,该研究揭示了小鼠核移植胚胎早期发育过程中多种组蛋白修饰的动态变化及其层级调控网络,为理解核移植效率低下的分子机制提供了新的思路。
同济大学生命科学与技术学院张晓蕾博士(现同济大学附属口腔医院)和徐睿敏博士为论文共同第一作者。同济大学生命科学与技术学院高绍荣院士、刘晓雨教授,同济大学附属妇产科医院李翀副研究员为论文共同通讯作者。该研究获得科技部、基金委及上海市科委、上海市教委等项目的资助。
论文链接:https://academic.oup.com/proteincell/advance-article/doi/10.1093/procel/pwaf010/8011356